耐热细菌蛋白酶的生物特性及其与胃蛋白酶和唾液淀粉酶的比较研究
在极端环境中生存的微生物一直是生物科学研究的焦点。科学家发现了一种耐热细菌,其适宜生存环境为温度90℃、pH为7.0。这种细菌不仅展现了出色的热稳定性,还从其体内成功提取出一种细菌蛋白酶。本文旨在探讨这种细菌蛋白酶的生物特性,并与人体消化系统中的胃蛋白酶及唾液淀粉酶进行对比分析。
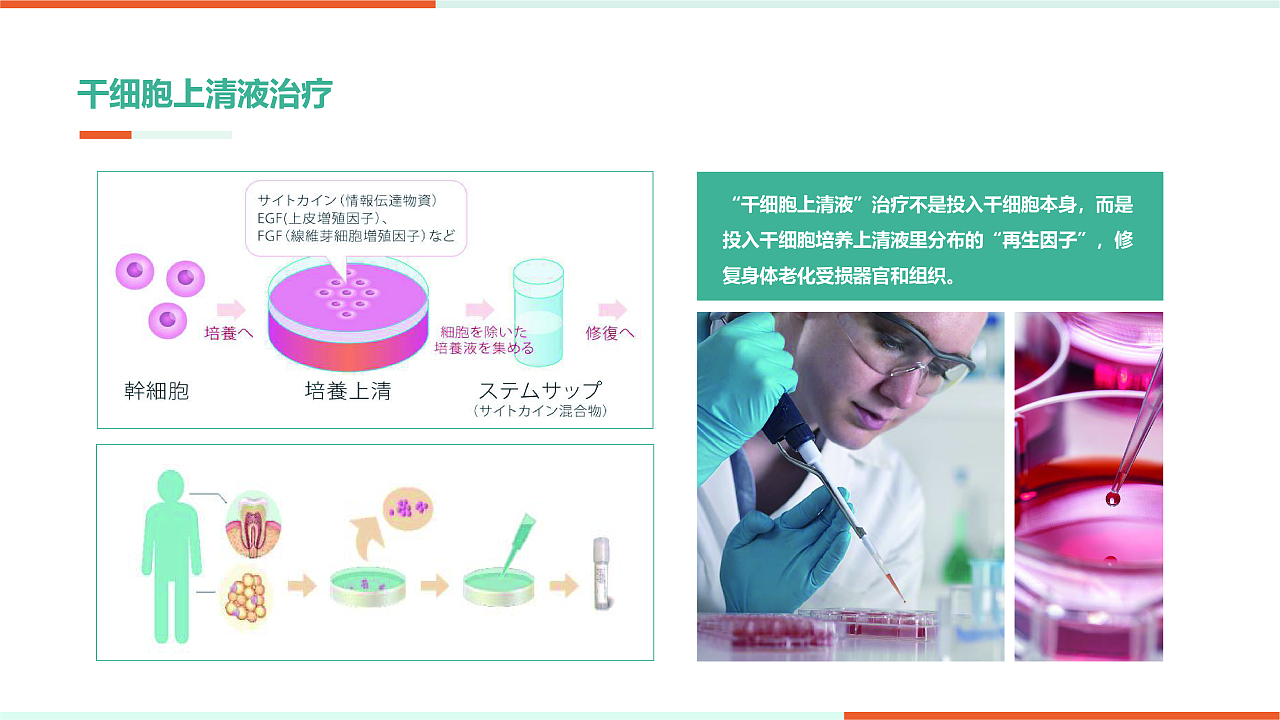
耐热细菌蛋白酶的发现与特性
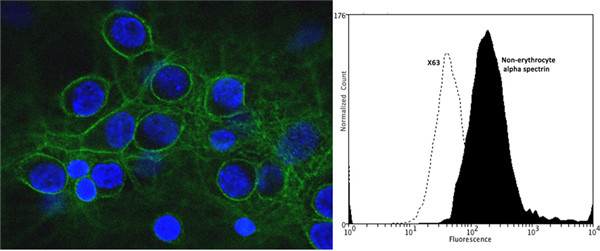
该耐热细菌能够在高温条件下生存,表明其体内酶系统具有极强的热稳定性。提取出的细菌蛋白酶在90℃和中性pH(7.0)环境中表现出高活性,这与常见的蛋白酶(如胃蛋白酶,最适pH为酸性)形成鲜明对比。这种蛋白酶可能通过独特的氨基酸序列和结构(如更多的二硫键或疏水相互作用)来维持高温下的构象稳定,使其在工业生物催化、洗涤剂生产及食品加工中具有潜在应用价值。
与胃蛋白酶和唾液淀粉酶的对比
- 胃蛋白酶:作为一种消化酶,胃蛋白酶在胃部的强酸性环境(pH约1.5-2.0)中活性最高,专门分解蛋白质为多肽。其热稳定性较低,通常在高温下易变性失活。相比之下,新发现的细菌蛋白酶在高温中性环境中更稳定,显示了不同的适应机制。
- 唾液淀粉酶:由唾液腺分泌,唾液淀粉酶在口腔中性环境中起作用,可将淀粉水解成麦芽糖和葡萄糖。其最适温度约为37℃,与人体体温一致,高温会导致快速失活。虽然唾液淀粉酶与细菌蛋白酶在pH偏好上有相似之处(均近中性),但细菌蛋白酶的热稳定性远高于唾液淀粉酶,凸显了极端微生物酶的独特性。
应用潜力与细胞培养考虑
这种耐热细菌蛋白酶在工业领域有广阔前景,例如在高温生物反应器中用于蛋白质降解或合成。在细胞培养研究中,蛋白酶常被用于细胞消化或培养基处理,但需注意其活性条件。细菌蛋白酶的高温需求可能限制其在常规细胞培养(通常37℃)中的应用,除非进行工程化改造以适应低温。未来研究可探索基因编辑技术,将该蛋白酶引入其他微生物或细胞系,以优化生产流程或开发新型生物工具。
结论
新发现的耐热细菌蛋白酶以其独特的热稳定性和中性pH活性,拓展了我们对酶适应性的理解。与胃蛋白酶和唾液淀粉酶的对比强调了环境对酶功能的塑造作用。进一步研究其结构和机制,将有助于开发创新应用,并可能推动合成生物学与工业生物技术的发展。
如若转载,请注明出处:http://www.dlyllx.com/product/20.html
更新时间:2026-04-17 00:43:59